Phương trình C3H4 + AgNO3 + NH3 → C3H3Ag + NH4NO3
1. Phương trình phản ứng hóa học
CH≡C-CH3 + AgNO3 + NH3 → AgC≡C-CH3 + NH4NO3
Bạn đang xem: C3H4 ra C3H3Ag l C3H4 + AgNO3 + NH3 → C3H3Ag + NH4NO3
2. Hiện tượng nhận biết phản ứng.
– Xuất hiện kết tủa màu vàng
3. Điều kiện phản ứng
– Không có
4. Bản chất của các chất tham gia phản ứng
C3H4 thuộc dạng ank-1-in có nguyên tử H liên kết trực tiếp với nguyên tử C liên kết ba đầu mạch có tính linh động cao hơn các nguyên tử H khác nên có thể bị thay thế bằng ion kim loại. (Chú ý: Phản ứng dùng để phân biệt ank-1-in với anken và các ankin khác)
5. Mở rộng tính chất hóa học của C3H4, AgNO3, NH3
5.1. Tính chất hóa học của AgNO3
– Mang tính chất hóa học của muối
a. Tác dụng với muối
AgNO3 + NaCl →AgCl↓+ NaNO3
2AgNO3 + BaCl2 →2AgCl↓+ Ba(NO3)2
b. Tác dụng với kim loại:
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
c. Tác dụng với axit:
AgNO3 + HI → AgI ↓ + HNO3
Oxi hóa được muối sắt (II)
Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag
5.2. Tính chất hóa học của C3H4
a. Phản ứng cộng
– Cộng brom
– Dẫn propin qua dung dịch brom màu da cam.
+ Hiện tượng: Dung dịch brom bị mất màu.
+ Propin có phản ứng cộng với brom trong dung dịch.
+ Sản phẩm mới sinh ra có liên kết đôi trong phân tử nên có thể cộng tiếp với một phân tử brom nữa:
+ Trong điều kiện thích hợp, propin cũng có phản ứng cộng với hiđro và một số chất khác.
– Cộng hiđro
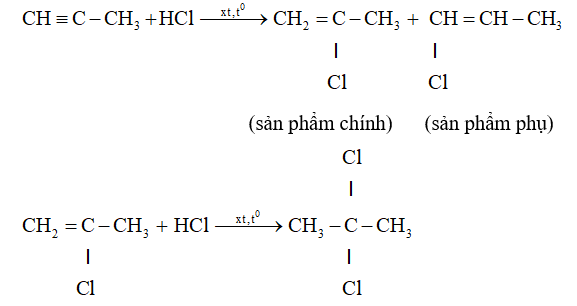
– Cộng hiđro clorua
+ Phản ứng cộng HX, H2O vào các ankin trong dãy đồng đẳng của axetilen cũng tuân theo quy tắc Mac-côp-nhi-côp như anken.
b. Phản ứng oxi hóa
– Propin là hiđrocacbon, vì vậy khi đốt, propin sẽ cháy tạo ra cacbon đioxit và nước, tương tự metan và etilen.
– Propin cháy trong không khí với ngọn lửa sáng, tỏa nhiều nhiệt.
c. Phản ứng thế bới kim loại
– Tính chất riêng của các ankin có nối ba đầu mạch
5.3. Tính chất hóa học của NH3
a. Tính bazơ yếu
– Tác dụng với nước:
NH3 + H2O ⇋ NH4+ + OH-
Xem thêm : HÓA CHẤT VIỆT QUANG
⇒ Dung dịch NH3 là một dung dịch bazơ yếu.
– Tác dụng với dung dịch muối (muối của những kim loại có hidroxit không tan):
AlCl3 + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4Cl
Al3+ + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4+
– Tác dụng với axit → muối amoni:
NH3 + HCl → NH4Cl (amoni clorua)
2NH3 + H2SO4 → (NH4)2SO4 (amoni sunfat)
b. Khả năng tạo phức
Dung dịch amoniac có khả năng hòa tan hiđroxit hay muối ít tan của một số kim loại, tạo thành các dung dịch phức chất.
Ví dụ:
* Với Cu(OH)2:
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2 (màu xanh thẫm)
* Với AgCl:
AgCl + 2NH3 → [Ag(NH3)2]Cl
Sự tạo thành các ion phức là do sự kết hợp các phân tử NH3 bằng các electron chưa sử dụng của nguyên tử nitơ với ion kim loại.
6. Cách thực hiện phản ứng
– Sục khí propin vào dung dịch hỗn hợp AgNO3/NH3
7. Bạn có biết
– Phản ứng trên gọi là phản ứng thế bằng ion kim loại
– Đây là phản ứng nhận biết ank – 1 – in
8. Bài tập liên quan (có đáp án)
Nguồn: https://thegioiso.edu.vn
Danh mục: Hóa